1. EvolvR: CRISPRゲノム編集ツール、超高速進化実験ツールへと進化
[出典]"CRISPR-guided DNA polymerases enable diversification of all nucleotides in a tunable window" Halperin SO, Tou CJ, Wong EB, Modavi C, Schaffer DV, Dueber JE. Nature. 2018 Aug 1
Innovative Genomics Institute@igisci
Fantastic IGI project out in @nature today: &vquot;CRISPR-guided DNA polymerases enable diversification of all nucleotide… https://t.co/vXKdadutIY
2018/08/02 02:40:59
EvolvR = nCas9–PolI3M
- Cas9のRuvCを変異(D10A)で不活性化したニッカーゼ改変型Cas9 (nCas9)で、gRNAで標的した二重鎖DNAの中のcrRNAに相補的なターゲット鎖を切断し、この一本鎖切断を、エラープローンなDNAポリメラーゼI変異体 PolI3M(PolI (D424A/I709N/A759R))で修復するEvolvRを開発
- gRNAを含むEvolvR発現プラスミドは、標的プラスミドのニック・サイトの3'端側17-ntの領域(ウインドウ)に置換誘導;
- 融合しない状態のnCas9とPolI3M、PolI3M単独、nCas9単独の場合は、置換は極めて稀か検出限界以下であり、fluctuation analysisにより測定した変異率においても同様の結果
変異率向上:enCas9-PolI5M
- Cas9の標的特異性を高める変異(K848A, K1003A, R1060A)*をnCas9に導入したenCas9と、PolIに3変異を導入したPolI3Mにさらに2変異(F742YとP796H)を導入したPolI5Mを融合することで、標的領域における変異率をnCas9–PolI3Mの33倍、野生型E. Coliの7,770,000倍にまで向上
- *) CRISPR関連文献メモ_2015/12/02 1."eSpCas9": Cas9/sgRBA/標的DNA三者複合体の構造に基づいて、オフターゲット編集を検出限界以下まで抑制するCas9変異体を作出
ウインドウ幅拡張:nCas9–PolI3M-TBD
- バクテリオファージT7由来のレドックス調節因子チオレドキシン結合タンパク質ドメイン(thioredoxin-binding domain, TBD)を結合することで、enCas9–PolI3Mの処理能力を向上し、ウインドウを17-ntから56-ntへと拡張
- EvolvRは細胞の生存性と増殖には影響を与えないことを確認
- 多重なgRNAを組み合わせた多重EvolvRも実証(同一鎖を標的とする場合は100-bp間隔のgRNAsペアを使用しても細胞致死に至らず)
応用例:抗生物質耐性変異予測
- 抗生物質スペクチノマイシン耐性をもたらす新たなリボソーム変異を同定:30Sリボソームのスペクチノマイシン結合ポケットを破壊する新規変異を、rpsE遺伝子を標的とするenCas9–PolI3M–TBDで探索し同定
2. ReMOT: 節足動物卵巣へCRISPR-Cas9 RNPを送達する新たな手法
- [出典]"Targeted delivery of CRISPR-Cas9 ribonucleoprotein into arthropod ovaries for heritable germline gene editing" Chaverra-Rodriguez D [..] Rasgon JL. Nat Commun. 2018 Aug 1.
- CRISPR-Cas9による節足動物の遺伝子編集はこれまでCas9 RNPの胚へのマイクロインジェクションにより行われてきたが、適用可能な種が限られており、また、適用可能な種の遺伝子編集も非効率であった。ペンシルベニア州立大の研究チームは今回、ReMOT (Receptor-Mediated Ovary Transduction of Cargo)法を開発し、ネッタイシマカ(Aedes aegypti)への遺伝性変異導入実験においてその有用性を実証した。
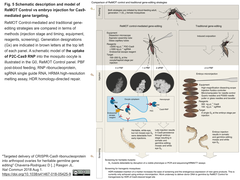 ReMOTは、卵黄形成の機構に基づいて、Cas9 RNPを卵黄タンパク質前駆体 (yolk protein precursors, YPP)由来のリガンド(D. melanogaster Yolk Protein 1 (DmYP1)由来のペプチド; P2Cと命名)に結合し、メスの血リンパへ注入し、卵母細胞へ送達する。胚へのマイクロインジェクションを回避し、極めて低コストで特別のトレーニングを必要としない。(右図:ReMOT法と胚マイクロインジェクション法の比較)。
ReMOTは、卵黄形成の機構に基づいて、Cas9 RNPを卵黄タンパク質前駆体 (yolk protein precursors, YPP)由来のリガンド(D. melanogaster Yolk Protein 1 (DmYP1)由来のペプチド; P2Cと命名)に結合し、メスの血リンパへ注入し、卵母細胞へ送達する。胚へのマイクロインジェクションを回避し、極めて低コストで特別のトレーニングを必要としない。(右図:ReMOT法と胚マイクロインジェクション法の比較)。
- 今後、種特異的・卵巣特異的リガンド-受容体の組み合わせを同定することで、ReMOTによる遺伝子編集を多様な種へ広げていくことが可能である。
- [出典]"Long noncoding RNA licensing of obesity-linked hepatic lipogenesis and NAFLD pathogenesis"Zhao XY [..] Lin JD. Nat Commun. 2018 Jul 30.
- 非アルコール性脂肪性肝疾患(nonalcoholic fatty liver disease, NAFLD/ナッフルディー)では、LXR-SREBP1cパスウエイの活性化を介して、脂肪合成が異常に亢進する。研究チームは今回マウスモデルにおいて、このパスウエイがlncRNAの一種Blnc1の肝発現の亢進によって活性化し、一方で、CRISPR/Cas9を介して肝臓特異的にBlnc1を不活性化することで、マウスが非アルコール性脂肪肝炎から保護されることを見出した。
コメント