[出典] "Mechanistic Insights into the cis- and trans-Acting DNase Activities of Cas12a" Swarts D, Jinek M. Mol Cell. 2019-01-10. (bioRixv. 2018-06-22)
Cas9とCas12aの比較
[共通する機序]
- CRISPR-Casシステムのクラス2に分類されているタイプⅡとタイプVサブタイプA (V-A)のエフェクターであるCas9とCas12a (旧Cpf1)は、いずれも、単一マルチドメインのヌクレアーゼであり、crRNAに相補的なプロトスペーサとPAM配列を認識して、標識DNAに結合し、標的DNAを切断する。
- 標的DNA結合にあたっては、DNA二本鎖プロトスペーサ領域において、相補的なcrRNAのセグメントが結合するDNA鎖 (標的鎖; target strand, TS)に結合してRNA-DNAヘテロ二量体を形成し、同時に、crRNAが結合しない非標的鎖 (non-target strand, NTS)がシフトし、いわゆるR-ループとよばれるコンフォメーションが出現する。このR-ループ形成がTSとNTS双方のcis-切断を触媒する。
- R-ループ関連crisp_bio記事:CRISPRメモ_2017/11/19 - 5. CRISPR-SpyCas9によるゲノム編集時のR-loop形成の動態を一分子FRET(smFRET)で解析
[異なる機序]
- PAM配列:SpyCas9は、プロトスペーサNTSの下流に隣接する5′-NGG-3′ PAMを認識するが、Cas12aオーソログはプロトスペーサNTSの上流に隣接する5′-TTTV-3′ PAMを認識する。Cas12aはまた、結合性は低いが5′-TTV-3′, 5′-TCTV-3′, 5′-TCCV-3′, および5′-CCCV-3′もPAMとして認識する。
- 二本鎖DNA (dsDNA) 切断機構:Cas9は、TSとNTSをそれぞれHNHドメインとRuvCドメインで切断し、その結果、PAMの近位に平滑末端または1塩基オーバーハングの二本鎖DNA切断 (DSBs)を誘導する。Cas12aは、TSとNTSのいずれもRuvCドメインで切断し、PAMから遠位に5'末端に長いオーバーハング (5~7 nt)を伴うDSBsを誘導する。ただし、Cas9もCas12aもin vitroでDSBsサイトに生じた末端DNAをトリムすることが見出されている。
- Cas12aは一本鎖DNA (ssDNA)も切断:Cas12aは、crRNAにガイドされるdsDNA切断に加えて、crRNAのTS鎖結合をトリガーとしてNTS単独(すなわち ssDNA)を配列非選択的にtrans-切断する。
Cas12aによるDNA切断の構造基盤と分子機構
- 先行研究により、Cas12aがN末端のRECローブとC末端のNUCローブがWEDドメインで連結された構造をとり、RECローブは2つのαヘリックスドメインREC1とREC2で、NUCローブはPAM相互作用 (PI)、ブリッジヘリックス (BH)、RuvCおよびNucドメインで構成されていることが明らかにされ、Cas12aが標的DNAを認識し標的DNAに結合する分子機構が明らかにされてきた。
- 著者らは今回Cas12aがDNase活性を示す分子機序を詳らかにすることを目的として、Francisella novicida U112 Cas12a (FnCas12a)とcrRNAおよびssDNAまたはdsDNAとの三者複合体のX線結晶構造解析と生化学的解析を行った。
- その上で、先行研究 (Jeon et al., 2018、Singh et al., 2018およびStrohkendl et al.) の知見との整合性を検討しながら、Cas12aがcis-およびtrans-に標的DNAを切断する分子機構の統合モデルを提案した (原論文Fig.6 モデル図参照;先行3研究については本記事文末のcrisp_bio記事リスト参照):
- Cas12aのWEDとPIドメインによるPAM認識から標的dsDNAの巻き戻しが始まり、crRNAのシード配列領域のTS結合を契機としてR-ループ形成が始まり、crRNA-TS DNAの結合進行とTS-NTS巻き戻しの同時進行の結果、R-ループが完成する。
- crRNA-TS DNAの二量体化によって誘導されるRECローブのコンフォメーション変化によって、NTS結合グルーブがTSから分離されたNTSをRuvCドメインの触媒サイトに誘導可能になり、NTSのcis-切断に至る (すなわち、RuvCドメインのDNase機能の活性化はPAM結合には依存しない)。
- 続いて、PAMから遠位でのTS-NTSの巻き戻しによってTSのRuvC触媒サイトへの接近が可能になりTSのcis-切断に至る。
- その後、PAM遠位のdsDNAはCas12a-crRNAから遊離する一方で、PAMの近位のdsDNAがCas12a-crRNA複合体に結合し続けることで、活性を発揮するコンフォメーションが維持され、NTSのssDNAのtrans-切断が実現する。
- すなわち、Cas12aとPAMの結合は、RuvCドメインのDNase活性化には関与しないが、NTSの変位(TSとNTSの分離)とR-ループ形成を誘導することで、標的dsDNAの認識と切断に決定的な役割を果たす。
構造データ
- 三者複合体PDB登録データ (本記事投稿時には公開待ち):6I1L (FnCas12a-crRNA-TS-only complex) : 6I1K (FnCas12a-crRNA-TS-NTS complex)
- JinekらのMol Cell, 2017論文からのPDF登録データ:5NG6 (Crystal structure of FnCas12a bound to a crRNA); 5NFV (Crystal structure of catalytically inactive FnCas12 mutant bound to an R-loop structure containing a pre-crRNA mimic and full-length DNA target)
関連crisp_bio記事
- Jeon et al., 2018 [CRISPRメモ_2018/07/19] - 3. CRISPR-Cas12a (Cpf1)のDNA標的探索とDNA切断を直接観察 (モデル図 Fig. 6を以下に引用)
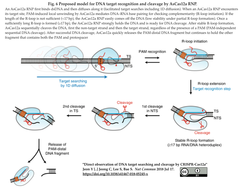
- Singh et al., 2018 [CRISPRメモ_2018/05/08 - 1] - 1. 一分子蛍光解析 (smFRET)と生化学的手法で、Cpf1 (Cas12a)と切断後の断片の振る舞いをリアルタイムで観察 (モデル図)
- Strohkendl et al., 2018 [CRISPRメモ_2018/07/02] - 5. CRISPR-Cas12aの標的DNA特異性が因って来たる速度論的基礎 (モデル図)
- CRISPRメモ_2018/08/23 - 4. [レビュー]Cas9とCas12a/Cpf1の比較
- CRISPRメモ_2018/05/20 - 6. [プロトコル]Francisella novicida由来Cas12a (Cpf1)のEscherichia coliでの発現と精製
コメント