2021-01-09 bioRxiv投稿以後にCell誌から刊行された論文へのリンクを追加
2020-05-25 初稿
-----------------------
[出典] "A natural single-guide RNA repurposes Cas9 to autoregulate CRISPR-Cas expression" Workman RE, Pammi T [..] Modell JW. (bioRxiv 2020-05-21) Cell 2021-01-08/2021-02-04; 184(3): P675-688.E19. https://doi.org/10.1016/j.cell.2020.12.017
タイプII CRISPR-Casシステムは、侵入DNA断片をスペーサとして格納してきたCRISPRアレイから転写されたCRISPR RNA前駆体 (pre-crRNA)が、トランスに転写されるlong-formとshort-form長短のcrRNA (tracrRNA)を足場として二本鎖RNAを形成し、バクテリア内在RNAse IIIによる切断を介して生成されるガイド鎖 (gRNA)へと成熟し、このgRNAがCas9を外来DNAにガイドし、Cas9が外来DNAを切断するに至る獲得免疫応答システムである。また、このgRNAを化学合成する発想 (sgRNA)によって、動植物としてヒトのゲノム編集が一気に広がることになった。
一方で、バクテリアとアーケアが、内在CRISPR-Casシステムが自己DNAを標的する自己免疫応答を回避する分子機構の解析が試みられ、これまでにいくつかのモデルが提案されてきた*。
[* 関連文献と記事]
[* 関連文献と記事]
- "Cost and Benefits of Clustered Regularly Interspaced Short Palindromic Repeats Spacer Acquisition" Bradde S, Mora T, Walczak AM. Philos Trans R Soc Lond B Biol Sci 2019-05-13 (PubMed PMC6452266); "How bacteria control the CRISPR-Cas arsenal" Leon LM, Mendoza SD, Bondy-Denomy J. Curr Opin Microbiol. Available online 21 November 2017. (PubMed PMC5899631)]。
- crisp_bio 2019-11-09 E. V. Kooninが「CRISPR生物学を巡る未解決問題」を提示してから1年余りが経過した
成果概要
JHUの研究グループは今回、S. pyogenes CRISPR-Casシステムをトランスポゾンを介して導入した Staphylococcus aureusへのファージ感染実験の結果に基づいて、本記事標題にあるように、全く新たな自己免疫応答抑制のモデルを提案した。
- Figure S1にあったlong tracrRNA (trL)が、crRNAとdsRNAを形成する足場として機能するだけでなく、trL自身がgRNAおよび人工のsgRNAと同様な形状へとフォールドし、この天然sgRNAがCas9のプロモーター (以下、Pcas9を抑制することでCas9の発現レベルが低下する [Figure 8引用モデル図 AとB参照]。
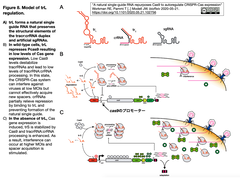
- このCas9発現抑制を介して、CRISPR-Cas9は、比較的少数のウイルスを排除するが、新たなスペーサ獲得には至らず、また、自己免疫応答も抑制される。
- trLが存在せずCas9プロモーター抑制が外れている状態では、新規ウイルスに対する免疫応答が3,000倍まで増強され、同時に、自己免疫応答のリスクも高まる。
- したがって、Pcas9が獲得免疫応答と自己免疫応答の双方を制御している。
- In silico解析は、このtracrRNAを介した制御が、タイプII CRISPR-Casシステム全般に拡がっていることを示した。
- CRISPRメモ_2018/08/22 5. RNAを標的とするタイプVI-A CRISPRにおいて自己ターゲッティングを回避するルールは?

コメント