1. ゲノム編集に対する国内議論
- [出典]"ゲノム編集 遺伝子残存なければ規制対象外に" NHK NEWS WEB 2018年8月20日 19時24分;英語版 "Govt. panel to not regulate some genome editing" NHK WORLD-JAPAN> NewsBiz / Tech 2018 Aug 21, 13:48.
- ゲノム編集の規制を議論していた国の検討会が打ち出した方針の概要とそれに対するバイオインダストリー協会や日本消費者連盟の反応を、ゲノム編集の解説と海外の動向も添えて、報道
2. 第2回ヒトゲノム編集国際サミット11月に香港大学で開催
- Second International Summit on Human Genome Editing
- November 27-29, 2018 The University of Hong Kong
- The Academy of Sciences of Hong Kong/The Royal Society/U.S. National Academy of Sciences/U.S. National Academy of Medicine
3. CRISPR-Cas9によるDBSはヘテロ接合を消失させオフターゲット変異を引き起こす
- [出典]"Allele-specific genome editing using CRISPR-Cas9 causes off-target mutations in diploid yeast" De Vries ARG [..] Daran JMG. (bioRxiv 2018 Aug 22) Nuclec Acids Res. 2019-02-20. https://doi.org/10.1093/nar/gky1216
- CRISPR-Cas9による遺伝子編集は、半数体とホモ接合型二倍体ゲノムでは極めて効率的であるが、多倍数性そしてまたはヘテロ接合型ゲノムでの効率は低い。デルフト工科大学の研究チームは今回、S. cerevisiaeとS. eubayanusのハイブリッドにおいて、ヘテロ接合のゲノム編集効率を体系的に分析した。
- ホモ接合型遺伝子座の編集効率に比べて個々のヘテロ接合型遺伝子座の編集効率は99分の1程度であった。
- 加えて、Cas9による二重鎖DNA切断(DSB)がヘテロ接合の大規模な欠失を誘導し、最大360-kbまでにおよぶゲノム領域に影響を与える。その結果、標的鎖がsgRNAの標的にならなかったホモログからの配列により置換され、ひいては、ほぼ1,700箇所のオフターゲット変異が誘導されることを、見出した。このヘテロ接合の消失パターンは、相同組換え修復過程と整合した。
- ヘテロ接合の消失は、抗腫瘍性やアポトーシス促進性のヘテロ接合遺伝子座における機能コピーの欠損が癌化を招くことから、ヒト遺伝子治療には特に有害な変異である。
4. In vivo CRISPR-Cas9を介した体細胞組換えにより、膵臓癌モデルマウスを迅速に作出するパイプラインを整備
- [出典]"A pipeline for rapidly generating genetically engineered mouse models of pancreatic cancer using in vivo CRISPR-Cas9 mediated somatic recombination" Ideno N [..] Ghosh B. bioRxiv. 2018 Aug 23.
- 膵管腺癌(pancreatic ductal adenocarcinoma、PDAC)の遺伝子改変マウスモデル(Genetically engineered mouse models, GEMMs)は、この悪性度の高い癌の発症機序の解明に有用な研究資源である。しかし、自発性PDAC GEMMsの開発は多大な経費、時間および人手を要する。また、これまでのPDAC GEMMsでは、ヒトのPDACと異なり、ドライバー・アレルの胚性膵臓全体にわたる活性化または損失が発生する。CRISPR/Cas9遺伝子編集によりこうした問題を解決できる可能性があるが、それには、in vivoでの編集効率を確保する必要がある。
- UT MD Anderson Cancer CenterとRice U.の研究チームは今回、膵臓でp48プロモーターによりCas9を発現する系統を基盤として、複雑なジェノタイプを帯びた自発性PDAC GEMMsを高効率で作出可能とするパイプラインを確立した。
- p48-Cre; LSL-Cas9マウスの膵臓に多重なsgRNAsをAAVで送達し、HDRを介した発癌性Kras G12Dアレルの発現と、癌抑制遺伝子(Trp53, Lkb1およびArid1A)のノックアウトを実現した。これによって得られたGEMMsは、膵上皮内腫瘍 (pancreatic intraepithelial neoplasia, PanIN)と膵管内乳頭粘液性腫瘍(Intraductal papillary mucinous neoplasm, IPMN)といった膵臓癌の前癌病変を示し、やがて、PDACへと進行した。
5. PAVOOC:タンパク質3次元構造と機能ドメイン・アノテーションに基づくCRISPR sgRNA設計
- [出典]"PAVOOC: Designing CRISPR sgRNAs using 3D protein structures and functional domain annotation" Schaefer M, Clevert DA, Weiss B, Steffen A. bioRxiv. 2018 Aug 23.
- PAVOOCは最先端の機械学習モデルに基づいてsgRNAsをランキングするWebベースのCRISPR sgRNA設計ツールである。PAVOOCは"Prediction And Visualization of On- and Off-targets for CRISPR"に対応する呼称である。
- 編集標的とする遺伝子(Gene of interest, GOI)の記号またはEnsemble IDを入力し、必要に応じて癌細胞株を選択すると、原論文Figure 1から引用した下図上段右上にある"LineUp"パネルに、機械学習モデルに基づいて算出したオンターゲットスコア(緑色)とオフターゲットスコア(赤色)に準じたランキングに応じて、GOI編集用sgRNAs候補が表示される。
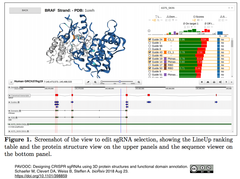
- この中から選択したsgRNA(s)について、上図上段左側のタンパク質立体構造上に切断部位が表示され、上図下段に癌細胞における変異を含むアノテーションが付されたゲノム地図が表示され、利用者は遺伝子/タンパク質の機能ドメインとの位置関係などを考察したより効果的なsgRNA(s)を選択可能になる。
- PAVOOCに組み込まれたアルゴリズムについては引用文献あり。
- Webサイト:https://pavooc.me
- チュートリアル(YouTube動画 6m19s) "PAVOOC Tutorial Part 1: sgRNA design for KO experiments" Schäfer M. 2018/06/13.
コメント