(創薬等PF・構造生命科学ニュースウオッチ 20160406)
- 小池亮太郎;太田元規(名古屋大学)
- [CPの構造]
- CPは、アクチンフィラメントの端に結合しアクチンの伸長を抑制し、アクフィンフォラメント量を調整するが、CP自身が、二種類のタンパク質V-1とCARMILによって調節される。
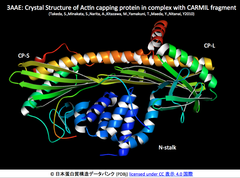
- CP/V-1複合体のCP/CARMIL複合体はそれぞれ解かれており(2挿入図参照)、V-1はCPとアクチンフィラメント端との阻害を直接阻害する部位に結合し、CARMILはアクチンフィラメント端結合部位とは異なる領域に結合することが明らかにされている。
- さらに、CARMILによるCPの阻害は、CPの構造全体を変形させるというよりは、CPの柔軟性(flexibility)の改変を介したアロステリック阻害機構によることが示唆されていた。
- 著者らは今回、CP単体、CP/CARMIL複合体およびCP/V-1複合体の分子動力学シミュレーションを行い、得られた軌跡を、タンパク質の領域を大小の剛体とみなしそれらの局所的動きから大領域に至るまでの動きを同定可能にするMotion Tree法で解析した。
- CARMILとV-1がCPの柔軟性に与える影響を、20種類の主要な剛体の動きで特徴付けることに成功し、CP調節の新たな機構を見出した。
- 単体のCPとCP/V-1複合体においては、N-stalkとCP-Sドメインの間隙周辺で頻繁にドメインが動いていたが、CARMILペプチドはこの間隙に結合することで、その動きを効果的に抑止していた。CARMILの間隙への結合はまた、V-1結合に関与するポケット周辺の局所的な動きを改変・亢進しており、V-1のCPへの結合を抑制することが示唆された。
- 論文→小池亮太郎(Ryotaro Kike)et al. “Comprehensive analysis of motions in molecular dynamics trajectories of the actin capping protein and its inhibitor complexes.” Proteins. 2016 Jul;84(7):948-56. Published online 2016 Apr 16.

コメント