2020-09-19 PNAS採択論文の書誌事項を追加
2019-05-29 bioRxiv投稿に準拠した初稿
[出典] "A CRISPR homing gene drive targeting a haplolethal gene removes resistance alleles and successfully spreads through a cage population" PNAS 2020-09-14 < "Resistance is futile: A CRISPR homing gene drive targeting a haplolethal gene" Champer J, Yang E [..] Messer PW. bioRxiv 2019-05-27.
[出典] "A CRISPR homing gene drive targeting a haplolethal gene removes resistance alleles and successfully spreads through a cage population" PNAS 2020-09-14 < "Resistance is futile: A CRISPR homing gene drive targeting a haplolethal gene" Champer J, Yang E [..] Messer PW. bioRxiv 2019-05-27.
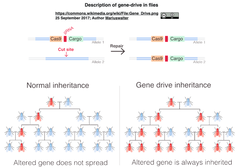
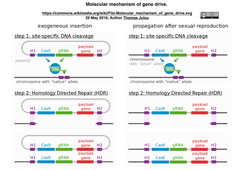
遺伝子ドライブはCas9を代表とするCRISPRエフェクターにより野生型遺伝子を切断し、その相同組み換え修復 (HDR)を介して、ドライブ・カセット (ひいてはドライブ・アレル)を野生型遺伝子に組み込むことで、ドライブ・アレルを自己伝播させていく技術である [左下図にショウジョウバエをモデルとする遺伝子ドライブの概要図を、右下図に遺伝子ドライブの分子機構モデル図を、Wikiipedieaから引用)。 ここで、DNA切断がHDRではなくNHEJで修復されると野生型遺伝子に変異が誘発され、その結果、遺伝子ドライブに組み込まれたgRNAの認識を免れる"遺伝子ドライブ抵抗性アレル"が生成される。ショウジョウバエにおいて、この抵抗性アレルが受精前の生殖細胞系列においても受精後の胚においても高頻度で生成されることが観察されている。
コーネル大学の研究グループは今回、ショウジョウバエにおいて、ハプロ致死性遺伝子を標的とする2種類のgRNAsとレスキュー・アレルを供するハプロ致死性ホーミングドライブ (Haplolethal Homing drive (以下、HHD))を設計し [原論文引用下図FIGURE2参照]、これによって、ドライブの高効率な継代と抵抗性アレルの抑制を、実現した。レスキュー・アレルは、gRNAによる認識を免れるように同義置換を多数導入した野生型配列 (図の中で紫色のrecoded配列)に由来する。
ハプロ致死性遺伝子を標的とすることで、NHEJ修復により変異が誘発されたアレル [上図FIGURE 1 黄色のバー]が致死をもたらし、一方で、ドライブ・アレルはレスキュー・アレルの存在によって本来の野生型アレルと対合し、ハプロ致死性も免れて継代され、遺伝子ドライブとしての機能を維持していく。
研究室ケージ内での実験では、HHDの継承率は91%におよび、抵抗性アレルの生成は、生殖細胞系列と胚でそれぞれ~10%と~31%であった。大型ケージの実験では数世代でドライブ・アレルが全てのケージ内のショウジョウバエ全てに拡がった。
研究室ケージ内での実験では、HHDの継承率は91%におよび、抵抗性アレルの生成は、生殖細胞系列と胚でそれぞれ~10%と~31%であった。大型ケージの実験では数世代でドライブ・アレルが全てのケージ内のショウジョウバエ全てに拡がった。
[遺伝子ドライブ関連文献とcrisp_bo記事]

- 抵抗性アレル発生に関連する文献:"Evolutionary dynamics of CRISPR gene drives" Noble C, Olejarz J, Esvelt KM, Church GM, Nowak MA. Sci Adv. 2017 Apr 5;3(4):e1601964 (右図はFigure 1から引用)
- 2019-01-26 哺乳類動物遺伝子ドライブの試み
- 2019-12-18 バクテリアを標的とする遺伝子ドライブシステムを開発、多コピーの薬剤耐性遺伝子座を効率的に不活性化
- 2017-05-04
- 2020-09-20

コメント