[注] ブログ記事タイトルは,コロンビア大学のNewsのタイトルに準拠
[出典] "A programmable encapsulation system improves delivery of therapeutic bacteria in mice" Harimoto T, Hahn J [..] Leong KW, Danino T. Nat Biotechnol. 2022-03-17. https://doi.org/10.1038/s41587-022-01244-y; News: Engineering an “Invisible Cloak” for Bacteria to Deliver Cancer Drugs. Columbia University. 2022-03-17. https://www.engineering.columbia.edu/news/bacteria-cloaking-cancer-therapy
[出典] "A programmable encapsulation system improves delivery of therapeutic bacteria in mice" Harimoto T, Hahn J [..] Leong KW, Danino T. Nat Biotechnol. 2022-03-17. https://doi.org/10.1038/s41587-022-01244-y; News: Engineering an “Invisible Cloak” for Bacteria to Deliver Cancer Drugs. Columbia University. 2022-03-17. https://www.engineering.columbia.edu/news/bacteria-cloaking-cancer-therapy
がんの治療法として生きているバクテリアの利用が試みられてるが,バクテリアのヒトに対する免疫原性と毒性が課題である.この課題は,リポ多糖 (LPS)といった表面抗原の欠失や,バクテリア表面を生体適合性のある分子でコートすることで解決可能であるが,こうしたスタティックな手法は,バクテリアの抗腫瘍性の失活や,細胞に導入後の制御が不可能になるといった別の課題を伴うことになる.こうした表面改変に対して,Columbia Universityの研究グループは今回,バクテリアの莢膜多糖体 (capsular polysaccharides, CAP)を改変することで,バクテリアと体内環境との相互作用をダイナミックに制御することに成功した.
- CAPは,バクテリア外膜をコートし,さまざまな環境からバクテリアを保護するバイオ・ポリマーであり,ヒト体内でさまざまな免疫因子からバクテリアを保護し,バクテリアの生存と定着に貢献する.
- CAP合成経路のsRNAノックダウン・スクリーニングをベースとして,CAPの発現をイソプロピルβ-D-チオガラクトピラノシド (IPTG)で誘導可能とした (iCAP) .

- 具体的には,プロバイオティクス大腸菌Nissle 1917 (以下,EcN)をベースとして,タンパク質発現誘導剤イソプロピルβ-D-チオガラクトピラノシド (IPTG)を利用して,iCAPを制御した[Fig.1引用右図参照].
- iCAPを備えたEcNは,CAP発現状態 (カプセル化状態)ではヒトの免疫を回避し,CAPを失うと,ヒト体内から効果的にクリアされる.また,iCAP-EcNに与えるIPTGの量によって,iCAP-EcNがヒト血中で生存できる時間を制御できる.
- iCAP-EcNの最大容量は野性型の10倍になり,また,マウスがんモデルにおける抗腫瘍効果が改善された.
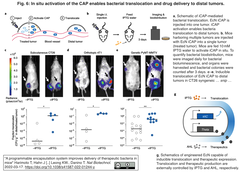
- さらに,IPTG存在下で抗腫瘍性のシータ毒素 (theta toxin, TT) を積荷とするiCAP-EcNを遠位腫瘍へと移動させ, IPTGと直交する誘導分子アシル化ホモセリンラクトン (AHL)に反応するluxIプロモーターを介してTTを発現するシステムを開発した [Fig. 6引用右図参照]
コメント